



多囊卵巢综合征(polycystic ovary syndrome, PCOS)作为育龄女性最常见的内分泌紊乱疾病之一,以高度异质性为特征。根据鹿特丹诊断标准,PCOS全球平均发病率高达15%,是导致女性不孕的首要原因之一。研究表明,除了卵泡自身的原因,卵巢颗粒细胞作为卵母细胞发育的"营养供给者",通过提供营养物质、激素及生长因子,对卵泡形成、发育及排卵过程发挥关键调控作用,其功能异常或死亡是卵泡闭锁及 PCOS 发生的核心病理诱因。
近年来,铁死亡作为一种铁依赖的非凋亡性细胞死亡形式,已被证实与PCOS、卵巢功能不全、子宫内膜异位症等多种女性生殖疾病密切相关。临床研究发现,PCOS 患者存在血清铁蛋白水平升高、转铁蛋白受体(TFRC)介导的铁摄取增加等特征,这些变化会促进活性氧(ROS)大量释放,引发脂质过氧化反应,最终导致颗粒细胞铁死亡。而铁死亡抑制剂能够有效改善 PCOS 相关病理改变,提示颗粒细胞铁死亡在卵泡发育停滞及 PCOS 发病中具有重要作用。然而,PCOS 状态下颗粒细胞铁死亡的上游调控机制,尤其是表观遗传层面的调控网络,至今尚未明确。
针对这一关键科学问题,江苏省解剖学会常务理事、南京大学医学院王勇教授团队开展了系统性研究,相关成果以 "Methylation reader MBD2-mediated GPX4 transcriptional repression drives ovarian granulosa cell ferroptosis in PCOS" 为题,于2026 年1月15日在国际权威期刊《Redox Biology》(IF=11.7)在线发表。

研究团队通过皮下注射脱氢表雄酮(DHEA)成功构建PCOS 小鼠模型,发现模型鼠卵巢组织中谷胱甘肽过氧化酶4(GPX4)——一种核心抗铁死亡酶 —— 表达显著下调,同时伴随TUNEL 阳性颗粒细胞增多、线粒体体积缩小、线粒体嵴结构消失等典型铁死亡形态学改变。为验证GPX4的功能重要性,团队构建了颗粒细胞特异性Gpx4 敲除小鼠(Gpx4GC-/-),发现敲除小鼠出现卵巢体积缩小、黄体比例降低、窦前卵泡累积、凋亡细胞增多等表型,铁死亡相关病理改变显著加剧;而通过药理学手段抑制GPX4活性,也得到了一致的结果,证实GPX4下调是驱动颗粒细胞铁死亡及卵巢功能异常的关键因素。
为探究PCOS 状态下GPX4 下调的分子机制,研究人员利用 MethPrimer 生物信息学工具分析发现,Gpx4 基因启动子区域存在密集的CpG 岛,为DNA 甲基化调控提供了结构基础。甲基化特异性PCR(MSP)和亚硫酸盐测序(BSP)实验进一步证实,PCOS 模型鼠卵巢组织中Gpx4启动子呈现明显的超甲基化状态。同时,模型鼠卵巢中DNA 甲基转移酶(DNMT1、DNMT3a、DNMT3b)及甲基化"阅读" 蛋白MBD2 表达选择性升高。重要的是,DNA 甲基转移酶抑制剂5 - 氮杂胞苷(5-Aza)能够有效逆转 DHEA 诱导的Gpx4 启动子超甲基化,恢复GPX4表达,明确了DNA甲基化在Gpx4转录抑制中的核心驱动作用。
为解析PCOS中Gpx4下调的转录抑制调控网路,研究团队对DHEA诱导的PCOS小鼠和对照小鼠卵巢组织进行了染色质开放性测序(ATAC-seq),发现Gpx4启动子转录起始区存在MAZ和MBD2的高亲和力结合位点(motif),且这些位点在在PCOS状态下调控活性显著增强。免疫共沉淀(Co-IP)和染色质免疫沉淀(ChIP)实验证实,MBD2在PCOS卵巢组织中可诱导性结合MAZ、HDAC3和NCoR,形成转录抑制复合物并聚集于甲基化的Gpx4 启动子区域。而MBD2选择性抑制剂KCC-07能够减少其在Gpx4 启动子上的结合,同时促进乙酰化的组蛋白(Pan-Ace)在该区域的富集,逆转GPX4低表达状态。这一发现揭示了MBD2 作为甲基化 "阅读" 蛋白,通过招募MAZ、HDAC3和NCoR转录抑制复合物促进组蛋白去乙酰化和染色质凝集,从而抑制Gpx4转录,最终诱发颗粒细胞铁死亡和卵巢损伤的分子机制。
为验证靶向该通路的治疗潜力,研究人员对PCOS 模型鼠分别给予MBD2 抑制剂KCC-07 和DNA 甲基转移酶抑制剂5-Aza 治疗。结果显示,两种药物均能有效恢复模型鼠卵巢组织中GPX4 的表达水平,降低脂质过氧化程度,显著改善卵巢纤维化和卵泡发育异常。提示MBD2促进GPX4转录抑制是PCOS卵巢铁死亡的重要表观遗传调控旁路。
为进一步确认GPX4 是MBD2 抑制剂发挥保护作用的关键靶点,团队在颗粒细胞特异性Gpx4 敲除小鼠(Gpx4GC-/-)和Gpx4fl/fl小鼠中构建 PCOS 模型并给予KCC-07 治疗。结果显示,KCC-07 能够有效改善DHEA诱导的野生型小鼠的卵巢功能障碍,但在Gpx4GC-/- 小鼠中,其抗铁死亡和卵巢保护作用均显著减弱,直接证实了KCC-07 的治疗效果依赖于对颗粒细胞GPX4 的恢复。
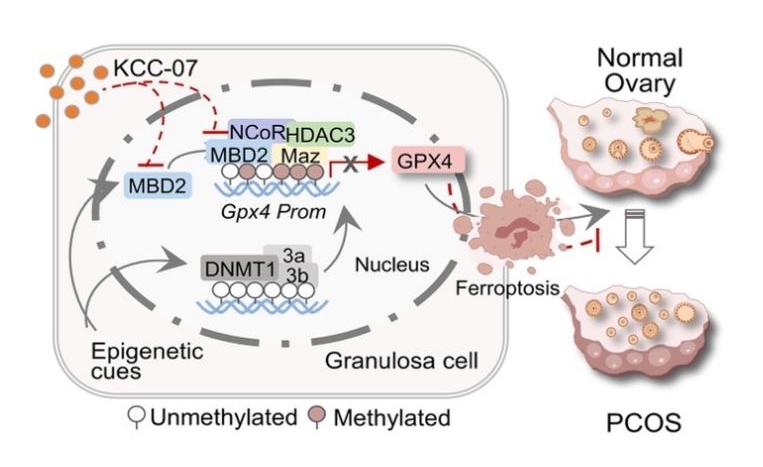
该研究首次揭示了MBD2 介导的表观遗传调控在 PCOS 颗粒细胞铁死亡中的核心作用,明确了 "MBD2/GPX4" 轴是驱动PCOS 卵巢病变的关键通路。这一发现不仅完善了PCOS 发病机制的理论体系,将表观遗传调控与铁死亡这两个重要生物学过程有机关联,更为临床治疗提供了全新的潜在靶点。与传统DNA 甲基转移酶抑制剂相比,靶向MBD2 的干预策略具有更高的特异性,能够在避免基因组广泛脱甲基化带来的脱靶毒性的同时,精准恢复GPX4 表达,为开发安全有效的PCOS 治疗药物提供了新思路和实验依据。
本研究得到国家自然科学基金(82471675、82201795、82470749)的资助。南京大学医学院曹望森教授、陶高见教授、王勇教授及王道娟助理研究员为论文共同通讯作者,研究生朱政全、王一涵为共同第一作者。
原文链接:https://doi.org/10.1016/j.redox.2026.104034
图文:南京大学医学院 王勇
编辑:吕海芹