



多囊卵巢综合征(Polycystic Ovarian Syndrome, PCOS)是生育期女性最常见的内分泌与代谢紊乱疾病,全球患病率高达8%–13%,以卵巢小窦卵泡增多、基质增生、颗粒细胞发育异常、排卵功能障碍及高雄激素血症为核心病理特征,卵巢纤维化与卵泡发育停滞是其关键病变表现。其中,雄激素受体(androgen receptor,AR)的是推动PCOS病理进程的重要核心机制,但其上游具体的表观遗传调控通路尚未被完全阐明。近日,江苏省解剖学会常务理事兼副秘书长、南京大学医学院王勇教授团队在Advanced Science(最新影响因子17.521)发表重要研究成果,首次揭示组蛋白乙酰转移酶p300通过特异性乙酰化组蛋白H3K18/H3K27,与转录因子SP1及乙酰化“阅读器”蛋白BRD4共同组装成转录激活复合体,直接驱动卵巢颗粒细胞中AR的转录活化,进而介导卵巢纤维化的发生发展,构成了PCOS发病的关键p300–SP1–BRD4表观遗传轴。该研究证实,通过遗传敲除或特异性药物抑制p300,可显著阻断AR的过度激活,有效改善PCOS模型小鼠的卵巢结构与功能异常,为PCOS的表观遗传靶向治疗开辟了全新方向。相关研究论文题为Identification of A p300–SP1–BRD4 Transcriptional Axis as a Key Driver of AR Hyperactivation in Polycystic Ovarian Syndrome,于2026年2月正式在线发表。

颗粒细胞AR过度激活,表观遗传调控成研究关键。既往研究已证实,即便在雄激素水平无显著升高的情况下,卵巢颗粒细胞中AR的持续激活仍是推动PCOS卵巢纤维化、卵泡发育受阻的核心因素,其通过介导氧化应激、慢性炎症、TGF‑β信号通路激活及胶原异常沉积等多种途径,破坏卵巢正常生理功能。AR的活性调控具有多层级特征,除受雄激素配体直接调控外,还受DNA甲基化、非编码RNA调控、蛋白/组蛋白乙酰化等表观遗传机制的精细调节。其中,组蛋白乙酰化介导的染色质构象改变,被认为是调控AR启动子转录活性、导致其在PCOS中持续激活的重要潜在机制,但其具体的调控分子与通路尚未明确,成为该领域的研究关键。
p300在PCOS中特异性上调,与AR激活及卵巢纤维化密切相关。为明确组蛋白乙酰转移酶在PCOS中的作用,研究团队构建了脱氢表雄酮(DHEA)皮下植入和高脂饮食饲喂两种经典的PCOS小鼠模型,病理检测发现模型小鼠卵巢均出现黄体数量显著减少、窦前卵泡比例升高、胶原大量沉积的典型纤维化表现,伴随排卵功能受损。蛋白水平检测显示,PCOS模型小鼠卵巢颗粒细胞中p300 与AR蛋白表达均显著上调,同时纤维化标志物α‑SMA和I型胶原(Col1α)表达升高,提示p300可能通过调控AR活化参与PCOS 卵巢纤维化进程。为验证该机制的临床相关性,研究团队整合了基因表达数据库(GEO)中15例PCOS患者与15例健康对照女性的卵巢颗粒细胞转录组数据,分析发现临床PCOS患者颗粒细胞中EP300与AR的mRNA表达均显著升高,且二者表达呈正相关,证实p300-AR轴的异常激活在临床PCOS中同样存在,为后续机制研究奠定了重要的临床基础。
p300介导H3K18ac/H3K27ac特异性乙酰化,精准驱动AR转录活化。组蛋白乙酰转移酶家族包含p300/CBP、Gcn5、MYST等多个亚家族,研究团队通过蛋白检测发现,在PCOS模型小鼠卵巢中,仅p300出现特异性显著上调,其余家族成员(CBP、Gcn5、Tip60、SRC3 等)表达无明显变化,且p300上调伴随组蛋白乙酰化修饰的特异性改变 —— 与基因启动子活化密切相关的H3K18ac、H3K27ac及H4K12ac、H4K16ac水平显著升高,而H4K5ac、H3K9ac等其他乙酰化标记无明显变化。体外功能实验进一步证实p300对AR的调控作用:利用p300激动剂CTPB处理原代卵巢颗粒细胞,可显著促进AR的蛋白表达;而采用p300特异性抑制剂A-485处理DHEA诱导的PCOS模型颗粒细胞,能以剂量依赖性方式显著下调H3K18ac/H3K27ac水平,并有效逆转DHEA诱导的AR上调,且A-485对H3K18ac/H3K27ac的抑制具有高度特异性,对H4K12ac、H4K16ac无明显影响。双荧光素酶报告基因实验则直接证实,p300抑制剂C646可显著抑制AR启动子的转录活性,明确p300通过调控AR启动子活性驱动其转录活化。
p300–SP1–BRD4形成转录复合体,构成AR激活的核心表观遗传轴。为解析p300调控AR转录的具体分子机制,研究团队采用ATAC-seq(染色质开放性测序)与 RNA-seq联合分析技术,发现PCOS模型小鼠卵巢中Ar基因启动子区域的染色质开放度显著增加,且与Ar mRNA 的表达上调高度一致,提示染色质构象开放是AR 转录活化的重要前提。对Ar启动子区域的转录因子结合基序分析发现,SP1结合位点的富集度最高,且PCOS模型小鼠卵巢中SP1的表达显著升高,ATAC-seq 足迹分析证实SP1在Ar启动子结合位点的占据能力显著增强,提示SP1是调控AR转录的关键转录因子。染色质免疫沉淀(ChIP)实验进一步证实,在PCOS模型小鼠卵巢及DHEA处理的颗粒细胞中,p300、SP1 与BRD4 共同富集于Ar启动子的SP1结合位点附近,且该区域伴随H3K18ac/H3K27ac的大量富集;而采用SP1抑制剂Plicamycin或p300抑制剂C646处理后,三者在Ar启动子的结合均显著减弱,同时AR的表达显著下调。免疫共沉淀(Co-IP)与多重免疫荧光实验进一步验证,在PCOS病理条件下,p300、SP1与BRD4在卵巢颗粒细胞的细胞核内形成稳定的转录激活复合体,且三者的异常共定位可被p300抑制剂C646有效破坏。报告基因突变实验则明确了该复合体的作用依赖于SP1结合位点:当将Ar启动子的SP1结合序列突变后,SP1过表达介导的AR启动子激活效应基本消失,且C646 或 Plicamycin对AR 启动子的抑制作用也显著减弱,证实p300–SP1–BRD4复合体通过结合Ar启动子的SP1位点,共同驱动AR的转录活化。
靶向抑制p300可重塑卵巢表观遗传环境,显著改善PCOS病理表型。为明确 p300在PCOS体内病理进程中的功能,研究团队构建了颗粒细胞特异性Ep300条件敲除小鼠(Ep300GC‑/‑),发现敲除小鼠在基础状态下卵巢形态与功能均正常,而在DHEA诱导的PCOS条件下,与野生型对照小鼠相比,Ep300GC‑/‑小鼠卵巢的黄体数量显著增多、胶原沉积明显减少,颗粒细胞中AR、α‑SMA和Col1α的表达水平显著降低,证实p300是介导PCOS中AR 激活与卵巢纤维化的必需分子。在体内药物干预实验中,研究团队分别在DHEA和高脂饮食诱导的两种PCOS模型小鼠中给予p300抑制剂C646,结果显示C646可有效恢复模型小鼠的发情周期规律性,降低小鼠体重、增加卵巢重量,同时显著提高卵巢黄体比例、减少窦前卵泡数量与胶原沉积;分子水平检测显示,C646可显著下调模型小鼠卵巢中p300、AR的表达,同时降低H3K18ac/H3K27ac及纤维化标志物Col1α、α‑SMA的水平,证实p300抑制剂可通过抑制p300-AR轴改善PCOS小鼠的卵巢功能异常。为进一步验证p300抑制剂的保护作用是否依赖于AR的抑制,研究团队在高脂饮食PCOS模型中联合给予AR激动剂DHT,结果发现DHT可显著削弱C646对卵巢纤维化的改善作用,同时逆转C646对AR及纤维化相关蛋白的下调效应,明确p300 抑制缓解PCOS病变的核心机制为阻断AR信号通路的过度激活。
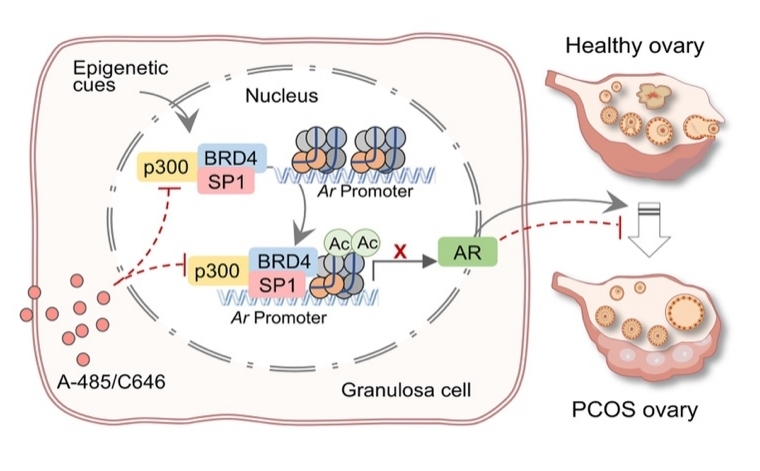
研究意义与潜在转化价值。该研究首次系统阐明了PCOS中卵巢颗粒细胞AR过度激活的表观遗传调控机制:p300通过选择性乙酰化H3K18/H3K27,与 SP1、BRD4在AR启动子区组装成转录激活复合体,驱动AR转录活化,进而介导卵巢纤维化与卵泡发育停滞,构成PCOS疾病特异性的p300–SP1–BRD4表观遗传轴。研究同时证实,EP300/Ep300与AR/Ar、SP1/Sp1的表达在临床PCOS患者颗粒细胞与小鼠PCOS卵巢中均呈高度正相关,且通过遗传敲除或特异性药物抑制p300,均可显著阻断AR过度激活,有效改善PCOS模型小鼠的病理表型。上述发现不仅丰富了PCOS表观遗传调控的理论体系,更首次将p300–SP1–BRD4–AR 轴确立为PCOS治疗的潜在核心靶点,为开发PCOS的表观遗传靶向药物提供了全新的分子靶点与实验依据,具有重要的理论意义与临床转化价值。
本研究得到了国家自然科学基金(82201795、82471675、82470749)的资助。南京大学医学院陶高见主任、曹望森教授、王勇教授和王道娟助理研究员为共同通讯作者;南京大学医学院博士研究生朱政全为第一作者。
原文链接:https://doi.org/10.1002/advs.202518185
供稿:王勇